|
 |
| 1996년 국제표준화기구 (ISO: International Organization for Standardization)는 1994년에 발행된 ISO 9000 시리즈(품질경영시스템)를 기본으로 의료기기 관련 산업분야를 특화한 ISO 13485/8 규격을 발행하였습니다. 기존 ISO 9000 품질경영시스템의 요구사항은 기존 의료기기 관련 산업분야의 특성을 충분히 반영하지 못하고 있기 때문에 좀더 특성화 되어 있는 품질경영시스템 규격의 필요성이 대두되었습니다. 특히, 의료기기 분야 산업은 인간의 생명과 직접적으로 연관되기 때문에, 제품의 잠재적인 불량은 바로 인간의 생명에 치명적인 영향을 미치게 되므로, 의료기기 산업 분야의 특성에 맞는 별도의 규격 제정은 당연한 것으로 여겨지고 있습니다. |
 |
 |
| ISO 13485/8의 목적은 기업이 품질경영시스템의 구축 및 실행을 통해 제품의 전과정을 시스템적으로 관리하고, 제품의 불량을 사전에 예방하며 또한 지속적으로 품질을 개선하여 고객 만족을 이루는데 목적이 있습니다. |
 |
| ISO 13485/8은 기존 ISO 9001/2의 요구사항을 모두 포함하며 의료기기 분야의 특성에 따른 추가적인 요구사항을 포함하는 구조로 구성되어 있습니다. 추가되는 요건을 예로 들면, 4.2.1 Technical File (DMR), 4.4 Clinical data, 4.4.1 Risk analysis, 4.4.4 Safety requirements등을 들 수 있습니다. |
 |
ISO 13485/8의 구축 및 실행을 통해 기업은 다음과 같은 효과를 기대할 수 있습니다.
|
 품질경영시스템을 통한 제품 전과정의 관리 품질경영시스템을 통한 제품 전과정의 관리
 사전 예방적 품질 관리와 지속적 품질 개선 사전 예방적 품질 관리와 지속적 품질 개선
 고객의 경영시스템 실행 요구사항의 안정적인 대응을 통한 매출증가 고객의 경영시스템 실행 요구사항의 안정적인 대응을 통한 매출증가
 전 종업원의 시스템적 접근 사고력 향상 전 종업원의 시스템적 접근 사고력 향상 |
|
 |
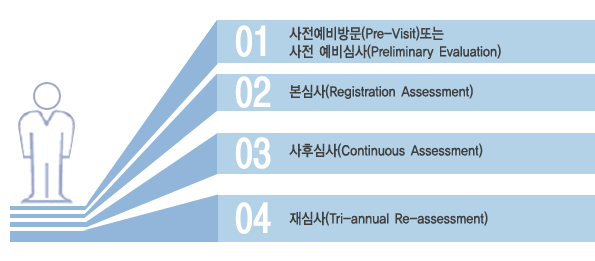
UL Korea는 ISO 13485/8 의료기기 분야 품질 경영시스템에 대한 고객의 요구를 만족시키기 위해 전문 심사원을 양성하여, ISO 13485/8 인증프로그램을 운영하고 있습니다. UL Korea는 전 세계 주요 의료기기 제조사에 대한 ISO 13485/8 인증을 통하여 제3자 인증기관으로서의 전문성과 권위를 인정 받았습니다. 특히 UL Korea의 심사원들은 실제 고객이 시스템을 구축하여 최대의 효과를 창출할 수 있도록 하는데 최선을 다하고 있습니다. UL 인증은 아래와 같은 형태로 구성되어 있습니다.
 |
|
|





